A. CACBON MONOXIT
I. TÍNH CHẤT VẬT LÍ
- CO là chất khí không màu, không mùi, không vị, ít tan trong nước, bền với nhiệt và rất độc.
- Kém hoạt động ở nhiệt độ thường, hoạt động nhiều hơn khi đun nóng
- CO là oxit trung tính
II. TÍNH CHẤT HÓA HỌC
- Phân tử CO có liên kết ba bền vững nên ở nhiệt độ thường C rất trơ, chỉ hoạt động trong điều kiện nhiệt độ cao.
- CO là oxit trung tính không có khả năng tạo muối → không tác dụng với dung dịch bazơ và dung dịch axit ở nhiệt độ thường.
1. Tính khử mạnh
- Tác dụng với oxi: cho ngọn lửa màu lam nhạt
2CO + O2 \(\xrightarrow{{{t}^{o}}}\) 2CO2
- Tác dụng với oxit kim loại:
Fe2O3 + 3CO \(\xrightarrow{{{t}^{o}}}\) 2Fe + 3CO2
2. Cacbon monoxit là oxit không tạo muối
III. ĐIỀU CHẾ
1. Trong phòng TN
HCOOH \(\xrightarrow{{{H_2}S{O_4}d,{t^{^o}}}}\) CO + H2
2. Trong công nghiệp
Cho hơi nước đi qua than nóng đỏ thu được khí than ướt
B. CACBON ĐIOXIT
I. TÍNH CHẤT VẬT LÍ
- CO2 là chất khí, không màu nặng hơn không khí, ít tan trong nước.
- Làm lạnh đột ngột ở -76oC, khí CO2 hóa thành khối rắn gọi là “nước đá khô”.
- Nước đá khô không nóng chảy mà thăng hoa.
II. TÍNH CHẤT HÓA HỌC
1. Tính chất của oxit axit
- Tác dụng với nước tạo thành dung dịch axit yếu.
CO2 (k) + H2O (l) ⇋ H2CO3 (dd)
- Tác dụng với oxit bazơ, bazơ tạo thành muối.
CO2 + NaOH → NaHCO3
2NaOH + CO2 → Na2CO3 + H2O
CaO + CO2 → CaCO3 (tº)
2. Tính OXH (Khi tác dụng với chất có tính khử mạnh)
2Mg + CO2 \(\xrightarrow{{{t}^{o}}}\) 2MgO + C
III. ĐIỀU CHẾ
1. Trong công nghiệp
C + O2 → CO2 (đốt cháy hoàn toàn than cốc trong không khí)
CaCO3 → CaO + CO2 (1000ºC)
2. Trong phòng thí nghiệm
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
C. AXIT CACBONIC VÀ MUỐI CACBONAT
I. AXIT CACBONIC
- Là axit kém bền, chỉ tồn tại trong dung dịch loãng, dễ bị phân hủy thành CO2 và H2O.
- Là axit hai nấc, trong dung dịch phân li hai nấc.
H2CO3 ⇋ H+ + HCO3-
HCO3- ⇋ H+ + CO32-
II. MUỐI CACBONAT
- Muối cacbonat của kim loại kiềm, amoni và đa số các muối hidrocacbonat đều tan tốt trong nước
- Muối cacbonat của các kim loại còn lại không tan, muối hidrocacbonat kếm bền nên dễ bị nhiệt phân
1. Tính chất hóa học
a) Tác dụng với axit:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
NaHCO3 + HCl → NaCl + CO2 + H2O
b) Tác dụng với dung dịch bazo:
NaHCO3 + NaOH → Na2CO3 + H2O
c) Phản ứng nhiệt phân:
2NaHCO3 → Na2CO3 + CO2 + H2O
CaCO3 → CaO + CO2
2. Nhận biết
Cho tác dụng với axit → CO2
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
3. Tính chất và ứng dụng của một số muối cacbonat
- Canxi cacbonat (CaCO3) tinh khiết là chất bột nhẹ, màu trắng, dùng làm chất dộn trong cao su và 1 số ngành công nghiệp.
- Natricacbonat (Na2CO3) khan (sođa khan) là chất bột màu trắng, tan nhiều trong nước. Dùng trong công ngiệp thủy tinh, đồ gốm, bột giặt, …
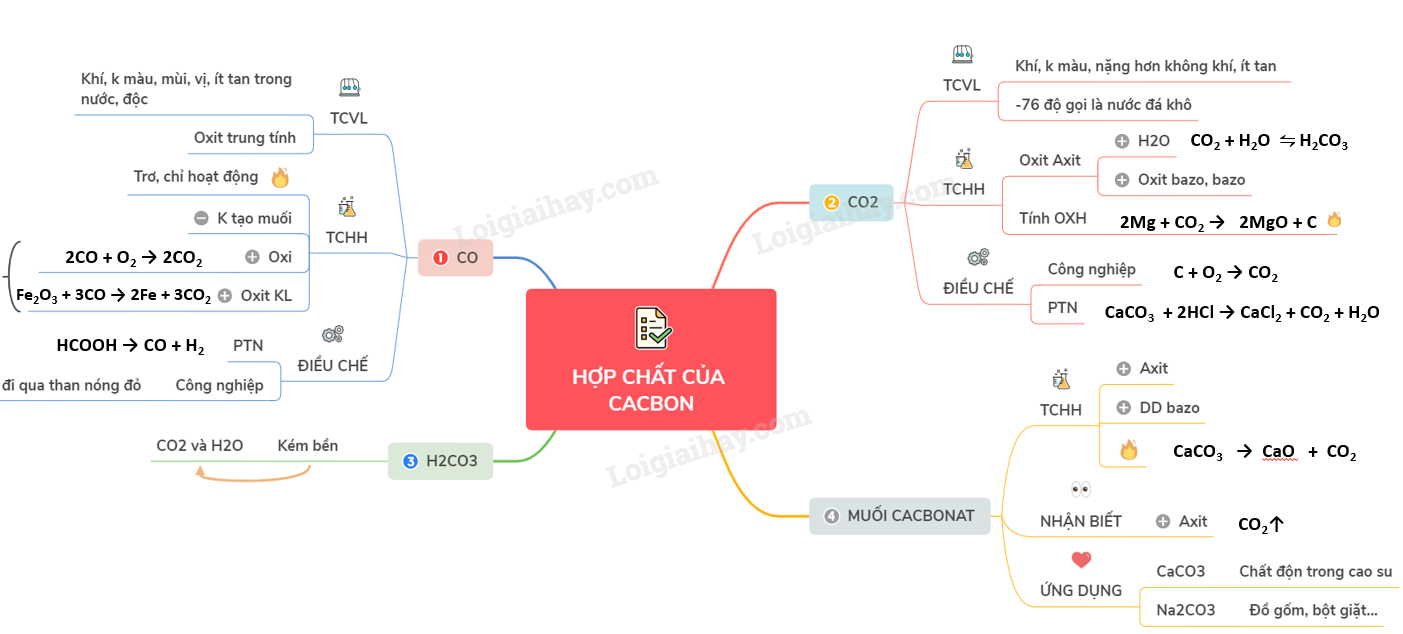
Sơ đồ tư duy: Hợp chất của cacbon
soanvan.me
