1. Thành phần hóa học
a. Sự phân hủy nước
- Khi cho dòng điện một chiều đi qua nước, trên bề mặt hai điện cực sinh ra khí hidro và oxi với tỉ lệ thể tích 2:1
PTHH: 2H2O \(\xrightarrow{{{\text{điện phân}}}}\) 2H2 + O2
b. Sự tổng hợp nước
- Đốt bằng tia lửa điện hỗn hợp 2 thể tích hidro và 2 thể tích oxi, ta thấy cuối cùng hỗn hợp chỉ còn 1 thể tích oxi. Vậy 1 thể tích oxi đã hóa hợp với 2 thể tích hidro tạo thành nước
PTHH: 2H2 + O2 \(\xrightarrow{{{t^o}}}\) 2H2O
c. Kết luận
- Nước là hợp chất tạo bởi 2 nguyên tố oxi và hidro. Chúng đã hóa hợp với nhau
- Bằng thực nghiệm, người ta tìm được CTHH của nước là H2O
2. Tính chất
a. Tính chất vật lí
- Là chất lỏng không màu (tuy nhiên lớp nước dày có màu xanh da trời), không mùi, không vị
- Sôi ở 100°C (p = 760 mmHg), hóa rắn ở 0°C
- Khối lượng riêng ở 4°C là 1 g/ml (hay 1kg/lít)
- Có thể hòa tan được nhiều chất rắn (muối ăn, đường,…), chất lỏng ( cồn, axit), chất khí (HCl,…)
b. Tính chất hóa học
- Tác dụng với kim loại: nước có thể tác dụng với một số kim loại ở nhiệt độ thường như Ca, Ba, K,…
PTHH: 2K + 2H2O → 2KOH + H2
- Tác dụng với mốt số oxit bazo như CaO, K2O,… tạo ra bazo tương ứng Ca(OH)2, KOH,…
+ Dung dịch bazơ làm quỳ tím chuyển xanh
VD: K2O + H2O → 2KOH
- Tác dụng với oxit axit như SO3, P2O5,… tạo thành axit tương ứng H2SO4, H3PO4,…
+ Dung dịch axit làm quỳ tím chuyển đỏ
VD: SO3 + H2O → H2SO4
3. Vai trò của nước và cách chống ô nhiễm nguồn nước:
- Vai trò
+ Hòa tan chất dinh dưỡng cho cơ thể sống
+ Tham gia vào quá trình hóa học trong cơ thể người và động vật
+ Có vai trò rất quan trọng trong đời sống: sản xuất công nghiệp, nông nghiệp, giao thông vân tải,…
- Cách chống ô nhiễm
+ Không vứt rác thải xuống nguồn nước
+ Xử lý nước thải trước khi cho nước thải chảy vào sông, hồ, biển.
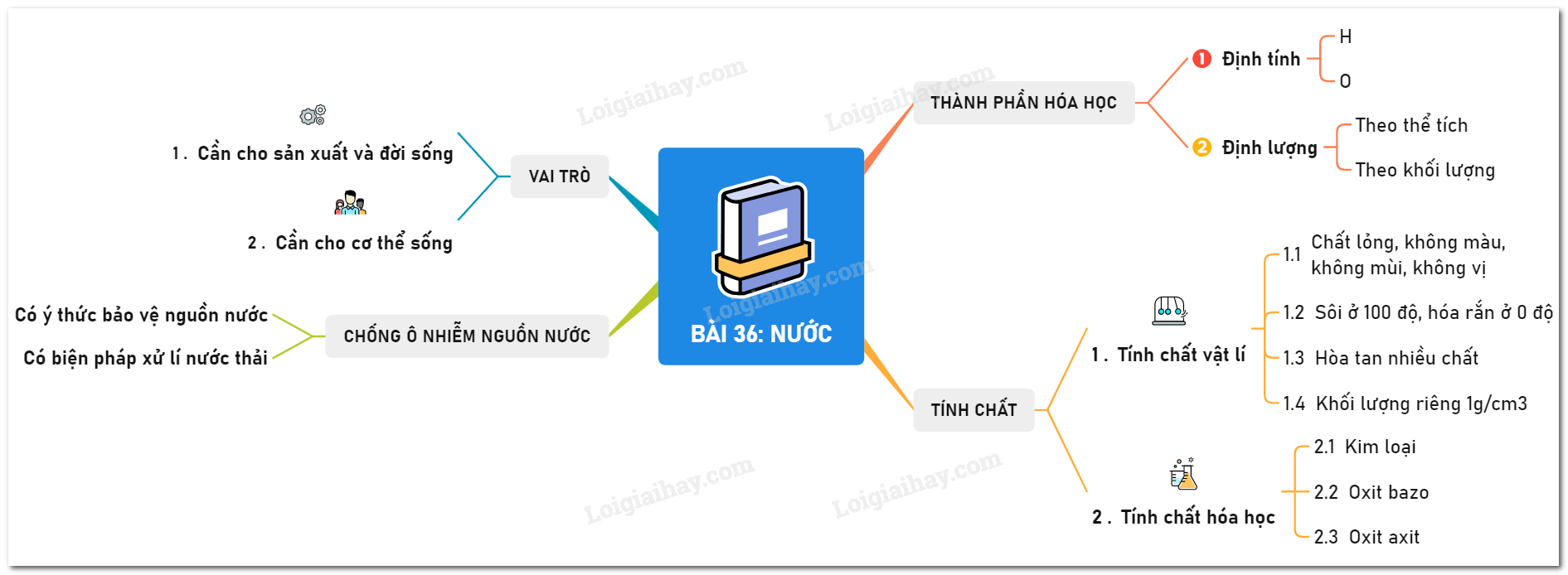
Sơ đồ tư duy: Nước