Lý thuyết về axit, bazơ và muối.
1. Theo thuyết A-rê-ni-ut
- Axit là chất khi tan trong nước phân li ra cation H+
Ví dụ: HCl → H+ + Cl-
- Bazơ là chất khi tan trong nước phân li ra anion OH-
Ví dụ : NaOH → Na+ + OH-
- Hiđroxit lưỡng tính là hiđroxit khi tan trong nước vừa có thể phân li như axit, vừa có thể phân li như bazơ.
Ví dụ : Zn(OH)2 \(\rightleftharpoons\) Zn2+ +2OH- ;
Zn(OH)2 \(\rightleftharpoons\) ZnO2-2 + 2H+
2. Axit nhiều nấc, Bazo nhiều nấc
- Những axit mà tan trong nước phân li nhiều nấc ra ion H+ gọi là các axit nhiều nấc.
Ví dụ : H2SO4, H3PO4....
H3PO4 \(\rightleftharpoons\) H+ + H2PO4–
H2PO4– \(\rightleftharpoons\) H+ + HPO42–
HPO42– \(\rightleftharpoons\) H+ + PO43–
- Những bazơ khi tan trong nước phân li nhiều nấc ra ion OH- gọi là các bazơ nhiều nấc. Ví dụ : Mg(OH)2, Ca(OH)2,....
Ví dụ:
Mg(OH)2 → Mg(OH)+ + OH-
Mg(OH)+ → Mg2+ + OH-
3. Muối
- Là hợp chất, khi tan trong nước phân li ra cation kim loại (hoặc cation NH4+) và anion gốc axit.
Ví dụ:
Na2CO3 → 2Na+ + CO32-
- Muối trung hòa là muối mà anion gốc axit không có khả năng phân li ra ion H+.
Ví dụ: NaCl, (NH4)2SO4…
- Muối axit là muối mà anion gốc axit có khá năng phân li ra ion H+.
Ví dụ: KHSO4, NaHCO3, NaH2PO4…
NaHSO4 → Na+ + HSO4-
HSO4- → H+ + SO42-
- Sự điện li cùa muối trong nước tạo cation kim loại (hoặc NH4+ , ion phức) và anion gốc axit.
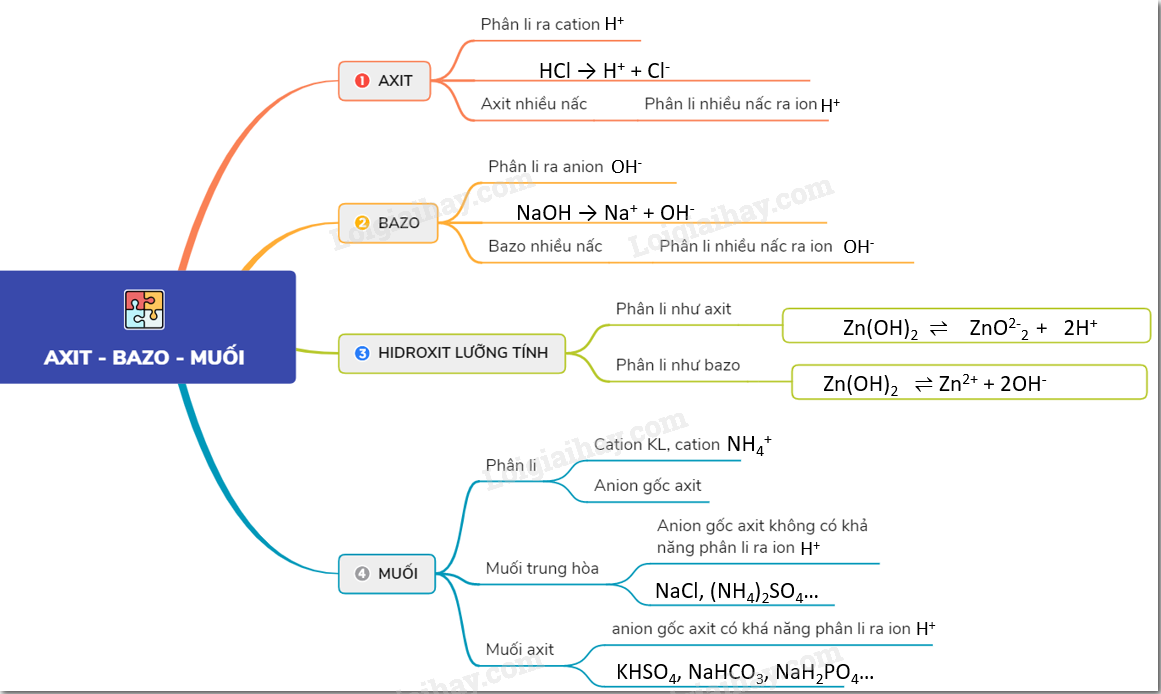
Sơ đồ tư duy: Axit, bazơ và muối.
soanvan.me
