Đề bài
Cho: H = 1; C = 12; O = 16; S = 32; N =14; P =15; F = 19; Cl = 35,5; Br = 80; I = 127; Li = 7; Na = 23; K = 39; Mg = 24; Ba = 137; Ca = 40; Cr = 52; Mn = 55; Fe = 56; Al = 27; Cu = 64; Ag = 108
Câu 41: Khi cho kim loại tác dụng với HNO3 thì không thể tạo ra hợp chất
A. N2O5. B. NH4NO3.
C. NO2 D. NO.
Câu 42: Cho m gam bột Fe vào 200ml dung dịch hỗn hợp A chứa H2SO4 1M, Fe(NO3)3 0,5M và CuSO4 0,25M. Khấy đều cho đến khi phản ứng kết thúc thoát ra khí NO và 0,75m gam hỗn hợp chất rắn. Giá trị của m là:
A. 32. B. 56
C. 33,6. D. 43,2.
Câu 43: Trên nhãn chai cồn y tế ghi “Cồn 700”. Cách ghi đó có ý nghĩa.
A. 100ml cồn trong chai có 70ml cồn nguyên chất.
B. Trong chai cồn có 70ml cồn nguyên chất.
C. Cồn này sôi ở 700 C.
D. 100ml cồn trong chai có 70 mol cồn nguyên chất.
Câu 44: Cho các phương trình hóa học sau (với hệ số tỉ lệ đã cho)
X(C4H6O4) + 2NaOH → Y + Z + T + H2O
T +4AgNO3 + 6NH3 + 2H2O → (NH4)2CO3 + 4Ag + 4NH4NO3
Z + HCl → CH2O2 + NaCl
Phát biểu nào sau đây đúng:
A. X là hợp chất tạp chức, có 1 chức axit và 1 chức este trong phân tử.
B. X có phản ứng tráng gương và làm mất màu brom.
C. Y có phân tử khối là 68.
D. T là axit fomic.
Câu 45: Cho các nhận định sau:
(1) Ở nhiệt độ thường, Cu(OH)2 tan được trong dung dịch glyxerol.
(2) Đốt cháy hoàn toàn axit oxalic thu được số mol CO2 bằng số mol H2O.
(3) Ở điều kiện thường, glyxylglyxin hòa tan được Cu(OH)2 tạo phức màu tím.
(4) Các α-aminoaxit đều có tính lưỡng tính.
Số nhận định đúng là:
A. 4. B. 3.
C. 2. D. 1.
Câu 46: Đốt cháy hoàn toàn một lượng hỗn hợp X chứa glucozơ và fructozơ, saccarozơ, mantozơ cân dùng vừa đủ 37,632 lít khí O2 (đktc) thu được CO2 và H2O. Cho toàn bộ sản phẩm cháy qua dung dịch Ba(OH)2 dư thấy có m gam kết tủa xuất hiện. Giá trị của m là
A. 260,04. B. 287,62.
C. 330,96. D. 220,64.
Câu 47: Đốt cháy hoàn toàn một ancol X thu được CO2 và H2O có tỉ lệ số mol tương ứng 3: 4. Thể tích khí oxi cần dùng để đốt cháy bằng 1,5 lần thể tích khí CO2 thu được (ở cùng điều kiện). Công thức phân tử X là
A. C3H8O2 B. C3H4O
C. C3H8O3 D. C3H8O
Câu 48: Chất có phản ứng màu biure là?
A. saccarozơ. B. tinh bột.
C. protein D. chất béo.
Câu 49: Hỗn hợp X gồm 0,15 mol CH4; 0,09 mol C2H2 và 0,2 mol H2. Nung nóng hỗn hợp X với xúc tác Ni thu được hỗn hợp Y. Cho hỗn hợp Y qua dung dịch brom dư thấy khối lượng dung dịch brom tăng 0,82 gam và thoát ra hỗn hợp khí Z. Tỷ khối của Z đối với H2 là 8. Thể tích của hỗn hợp Z( đktc) là
A. 5,6 lít. B. 5,824 lít.
C. 6,048 lít. D. 5,376 lít.
Câu 50: Cho 13,4 gam hỗn hợp X gồm hai axit no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồn đẳng tác dụng với Na dư, thu được 17,8 gam muối. Khối lượng của axit có nguyên tử cacbon ít hơn có trong X là
A. 4,6 gam. B. 7,4 gam.
C. 6,0 gam. D. 3,0 gam.
Câu 51: Để nhận biết ion NH4 + trong dung dịch, thuốc thử cần dùng là
A. dung dịch NaNO3
B. dung dịch NaOH.
C. dung dịch NH3.
D. dung dịch H2SO4.
Câu 52: Hòa tan hoàn toàn hỗn hợp rắn gồm Fe3O4 (1,2x mol) và Cu ( x mol) vào dung dịch HCl ( vừa đủ), kết thúc phản ứng chỉ thu được dung dịch X. Thêm dung dịch chứa 7,6 gam MgCl2 vào X, được dung dịch Y. Điện phân dung dịch Y đến khi nước bắt đầu điện phân ở anot thì ngừng điện phân, khi đó khối lượng dung dịch Y giảm 71,12 gam. Khối lượng muối khan thu được khi cô cạn dung dịch Y là
A. 54,80 gam. B. 60,64 gam.
C. 73,92 gam. D. 68,24 gam.
Câu 53: Hỗn hợp X gồm anđehit Y, axit cacboxylic Z và este T ( Z và T là đồng phân). Đốt cháy hoàn toàn 0,2 mol X cần 0,625 mol O2, thu được 0,525 mol CO2 và 0,525 mol nước. Cho một lượng Y bằng lượng Y có trong 0,2 mol X tác dụng với một lượng dư dung dịch AgNO3 trong NH3, đun nóng, sau phản ứng được m gam Ag ( hiệu suất phản ứng 100%). Giá trị của m là
A. 32,4. B. 16,2.
C. 64,8. D.21,6.
Câu 54: Phát biểu khống đúng là
A. Chất béo tan nhiều trong dung môi hữu cơ.
B. Dầu ăn và dầu bôi trơn máy có cùng thành phần nguyên tố.
C. Chất béo không tan trong nước, nhẹ hơn nước.
D. Chất béo là trieste của glixerol và axit béo.
Câu 55: Một vật làm bằng hợp kim Zn- Fe đặt trong không khí ẩm sẽ bị ăn mòn điện hóa. Các quá trình xảy ra tại điện cực là:
A. Anot: Fe→ Fe2+ + 2e và Catot: O2 + 2H2O +4e → 4OH-.
B. Anot: Zn→ Zn2+ + 2e và Catot: Fe + 2e → Fe2+ .
C. Anot: Fe→ Fe2+ + 2e và Catot: 2H+ + 2e → H2.
D. Anot: Zn→ Zn2+ + 2e và Catot: O2 + 2H2O + 4e → 4OH-.
Câu 56: Phát biểu nào sau đây đúng?
A. Tất cả các amin đều làm quỳ tím ẩm chuyển màu xanh.
B. Ở nhiệt độ thường, tất cả các amin đều tan nhiều trong nước.
C. Các amin đều không độc, được sử dụng trong chế biến thực phẩm.
D. Để rửa sạch ống nghiệm có dính anilin, có thể dùng dung dịch HCl.
Câu 57: Axit acrylic (CH2=CH-COOH) không tham gia phản ứng với
A. H2/xt. B. dung dịch Br2.
C. NaNO3. D. Na2CO3.
Câu 58: 227877 Cho hỗn hợp 2 aminno axit no chứa một chức –COOH và một chức –NH2 tác dụng với 110ml dung dịch HCl 2M, thu được dung dịch X. Để tác dụng hết với các chất trong X cần dùng 140ml dung dịch KOH 3M. Tổng số mol hai amino axit là
A. 0,2. B. 0,4
C. 0,1. D. 0,3.
Câu 59: Thủy tinh hữu cơ plexiglas là loại chất béo rất bền, trong suốt, có thể cho gần 90% ánh sáng truyền qua nên được sử dụng làm kính ô tô, máy bay, kính xây dựng, kính bảo hiểm, …Polime dùng để chế tạo thủy tinh hữu cơ có tên gọi là
A. poli(metyl metacrylat).
B. poli acrilonitrin.
C. poli(etylen terephtalat).
D. poli(hexametylen ađipamit).
Câu 60: Để phân biệt axit fomic và axetic có thể dùng
A. CaCO3
B. Cu(OH)2 ở điều kiện thường.
C. Dung dịch NH3.
D. AgNO3 trong dung dịch NH3.
Câu 61: Phát biểu không đúng là:
A. Sắt có trong hemoglobin (huyết cầu tố) của máu.
B. Phèn chua được dùng để làm trong nước.
C. Nước chứa nhiều HCO3 là nước cứng tạm thời.
D. Trong tự nhiên, các kim loại kiềm chỉ tồn tại ở dạng hợp chất.
Câu 62: Để loại bỏ khí CO2 có lẫn trong hỗn hợp CO và CO2, ta dẫn hỗn hợp khí qua
A. dung dịch Ca(OH)2.
B. dung dịch HCl.
C. dung dịch NaCl.
D. dung dịch H2O.
Câu 63: Hợp chất nào dưới đây không thể tham gia phản ứng trùng hợp.
A. Axit - aminocaproic.
B. Caprolactam.
C. Buta- 1,3- ddien.
D. Metyl metacrylat.
Câu 64: Đường fructozơ có nhiều trong mật ong, ngoài ra còn có trong các loại hoa quả và rau xanh như ổi, cam, xoài, rau diếp xoắn, cà chua….rất tốt cho sức khỏe. Công thức phân tử của fructozơ là
A. C6H12O6. B. C6H10O5.
C.CH3COOH. D. C12H22O11.
Câu 65: Trong phân tử của cacbohidrat luôn có
A. Nhóm chức xeton
B. Nhóm chức axit
C. Nhóm chức ancol
D. Nhóm chức andehit
Câu 66: Quặng boxit dùng để sản xuất kim loại
A. Mg B. Cu
C. Na D.Al
Câu 67: Cho sơ đồ phản ứng:

Công thức của T là:
A. CH3COOH
B. CH3COOC2H5
C. C2H5COOH
D. C2H5COOCH3
Câu 68: Cho hỗn hợp chất rắn X gồm Al, Zn và Fe vào dung dịch CuCl2. Sau khi phản ứng xong được hỗn hợp rắn Y và dd Z. Thêm dung dịch NaOH dư vào dung dịch Z thấy xuất hiện kết tủa T. Vậy rắn Y có thể gồm:
A. Zn, Fe, Cu B. Al, Zn, Fe, Cu
C. Fe, Cu D. Zn, Cu
Câu 69: Dung dịch E chứa các ion: Ca2+, Na+, HCO3-, Cl- trong đó số mol của Cl- gấp đôi số mol của ion Na+. Cho một nửa dung dịch E phản ứng với dd NaOH dư thu được 4g kết tủa. Cho một nửa dd E còn lại phản ứng với dd Ca(OH)2 dư thu được 5g kết tủa. Mặt khác, nếu đun sôi đến cạn dung dịch E thu được m gam chất rắn khan. Giá trị của m là:
A. 11,84 B. 8,79
C. 7,52 D. 7,09
Câu 70: Hòa tan hoàn toàn hỗn hợp gồm canxi cacbua và nhôm cacbua trong dung dịch HCl thu được hỗn hợp khí gồm:
A. C2H2 và H2
B. CH4 và C2H6
C. CH4 và H2
D. C2H2 và CH4
Câu 71: Muốn bảo quản kim loại kiềm người ta ngâm chúng trong
A. Dầu hỏa B. Xút
C. Ancol D. Nước cất
Câu 72: Trong các thí nghiệm sau
(1) Cho dung dịch H2SO4 phản ứng với dung dịch Ba(HCO3)2
(2) Cho dung dịch Na2CO3 vào dung dịch AlCl3
(3) Cho Ba vào dung dịch NaHSO3
(4) Cho Mg vào dung dịch NaHSO4
(5) Cho dung dịch NaHCO3 vào dung dịch Ca(OH)2
(6) Cho Na vào dung dịch CuSO4
Số thí nghiệm vừa có khí bay ra vừa có kết tủa là:
A. 5 B. 4
C. 2 D. 3
Câu 73: Dung dịch làm quỳ tím chuyển sang màu đỏ là:
A. CH3NH2 B. CH3COOH
C. CH3COOC2H5 D. C2H5OH
Câu 74: Dãy các chất làm nhạt (mất) màu dung dịch KMnO4 ở nhiệt độ thường là:
A. Toluen, buta – 1,2 – dien, propin
B. Etilen, axetilen, butadien
C. Benzen, toluen, stiren
D. Benzen, etilen, axetilen
Câu 75: Chất có nhiệt độ sôi thấp nhất là:
A. CH3COOH B. C6H5NH2
C. C2H5OH D. HCOOCH3
Câu 76: Cho CH3CH2CHO phản ứng với H2 (xúc tác Ni, đun nóng) thu được
A. CH3CH2OH
B. CH3CH2CH2CH2OH
C. CH3COOH
D. CH3OH
Câu 77: Hòa tan hoàn toàn hổn hợp A gồm Zn, ZnO với tỷ lệ số mol tương ứng là 4:3 vào dung dịch chứa 1,62 mol HCl, 0,19 mol NaNO3, kết thúc phản ứng thu được dung dịch X chỉ chứa muối và hỗn hợp khí Y gòm hai khí trong đó có một khí hóa nâu ngoài khống khí, tỷ khối của Y so với He là 6,1. Cố cạn dung dịch X thu được m gam muối khan. Tính m:
A. 107,92 B. 103,55
C. 99,7 D. 103,01
Câu 78:
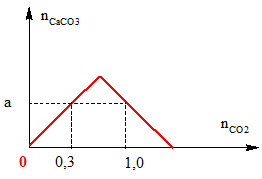
Sục từ từ đến dư CO2 vào một cốc đựng dung dịch Ca(OH)2. KQ thí nghiệm được biểu diễn trên đồ thị như hình bên. Khi lượng CO2 đã sục vào dung dịch là 0,85 mol thì lượng kết tủa đã xuất hiện là m gam. Giá trị của m là
A. 40 gam. B. 55 gam.
C. 45 gam. D. 35 gam
Câu 79: Peptit X và peptit Y có tổng số liên kết peptit bằng 8. Thủy phân hoàn toàn X cũng như Y đều thu được gly và Val. Đốt cháy hoàn toàn hỗn hợp E chứa X và Y có tỉ lệ số mol tương ứng là 1 : 3 cần dùng 22,176 lít khí O2 (đktc). Sản phẩm cháy gồm CO2, H2O và N2. Dẫn toàn bộ sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 46,48g. Khí thoát ra có thể tích 2,464 lít (đktc). Thủy phân hoàn toàn hỗn hợp E thu được a mol Gly và b mol Val. Tỉ lệ a : b là
A. 1 : 2 B. 1 : 1
C. 2 : 1 D. 2 : 3
Câu 80: Phương pháp chung để điều chế Na, Ca, Al trong công nghiệp là:
A. Thủy luyện
B. Nhiệt luyện
C. Điện phân dung dịch
D. Điện phân nóng chảy
Lời giải chi tiết
| 1 | 2 | 3 | 4 | 5 |
| A | D | A | B | C |
| 6 | 7 | 8 | 9 | 10 |
| C | D | C | C | C |
| 11 | 12 | 13 | 14 | 15 |
| B | D | B | B | D |
| 16 | 17 | 18 | 19 | 20 |
| D | C | A | A | D |
| 21 | 22 | 23 | 24 | 25 |
| C | A | A | A | C |
| 26 | 27 | 28 | 29 | 30 |
| D | B | C | A | D |
| 31 | 32 | 33 | 34 | 35 |
| A | B | B | B | D |
| 36 | 37 | 38 | 39 | 40 |
| B | D | C | B | D |
Xem thêm: Lời giải chi tiết Đề thi thử THPT Quốc gia môn Hóa học tại Tuyensinh247.com
soanvan.me
