Câu hỏi 1 :
Cộng hoá trị của 1 nguyên tố là:
- A Số e tham gia liên kết của nguyên tử của nguyên tố đó.
- B Số thứ tự nhóm của nguyên tử.
- C Hoá trị cao nhất của nguyên tố.
- D Số liên kết của nguyên tử nguyên tố đó trong phân tử.
Đáp án: D
Lời giải chi tiết:
Cộng hoá trị của 1 nguyên tố là số liên kết của nguyên tử nguyên tố đó trong phân tử.
Câu hỏi 2 :
Nhận định nào sau đây là đúng về điện hoá trị:
- A
Trong hợp chất ion, hoá trị của một nguyên tố bằng tích của điện tích và chỉ số của ion đó.
- B
Trong hợp chất ion, hoá trị của một nguyên tố bằng điện tích của ion đó.
- C
Điện hoá trị luôn là số dương và được viết số trước dấu sau.
- D
Điện hoá trị luôn là số âm và được viết số trước dấu sau.
Đáp án: B
Phương pháp giải:
Trong hợp chất ion, hóa trị của một nguyên tố bằng điện tích của ion và được gọi là điện hóa trị của nguyên tố đó.
Lời giải chi tiết:
Trong hợp chất ion, hóa trị của một nguyên tố bằng điện tích của ion và được gọi là điện hóa trị của nguyên tố đó.
=> Nhận định đúng về điện hóa trị là: B
Câu hỏi 3 :
Kiểu liên kết tạo nên giữa hai nguyên tử bằng một hay nhiều cặp electron chung được gọi là
- A liên kết cộng hóa trị.
- B liên kết ion.
- C liên kết hidro.
- D liên kết kim loại.
Đáp án: A
Lời giải chi tiết:
Liên kết cộng hóa trị được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung.
Câu hỏi 4 :
Ion nào là ion đơn nguyên tử?
- A NH4+
- B NO3-
- C Cl-
- D OH-
Đáp án: C
Phương pháp giải:
Ion đơn nguyên tử là ion được cấu tạo từ 1 nguyên tử.
Lời giải chi tiết:
Cl- là ion đơn nguyên tử.
Câu hỏi 5 :
Để đạt đến trạng thái bền vững theo quy tắc bát tử, nguyên tử Al cần
- A
nhường đi 3e.
- B
nhận vào 5e.
- C
nhường đi 1e.
- D
nhận vào 7e.
Đáp án: A
Lời giải chi tiết:
Cấu hình e của Al: 1s22s22p63s23p1
=> nguyên tử Al cần cho 3e để đạt cấu hình bền vững của Ne (1s22s22p6)
Câu hỏi 6 :
Cho dãy các chất : N2, H2, NH3, CO2, HCl, H2O, C2H4. Số chất mà phân tử chỉ chứa liên kết đơn là :
- A 4
- B 3
- C 1
- D 2
Đáp án: A
Lời giải chi tiết:
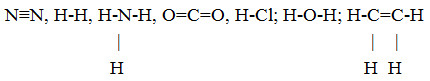
Các chất chỉ chứa liên kết đơn là: H2, NH3, HCl, H2O
Câu hỏi 7 :
Liên kết ion là liên kết được hình thành bởi
- A lực hút tĩnh điện giữa các ion trái dấu.
- B các electron độc thân.
- C các electron dùng chung.
- D các electron tự do.
Đáp án: A
Lời giải chi tiết:
Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Câu hỏi 8 :
Cho các ion: Na+, Mg2+, Al3+, Ca2+, S2-, Cl-, O2-. Số ion có 10e là:
- A
2.
- B
3.
- C
4.
- D
5.
Đáp án: C
Phương pháp giải:
+) Xác định số e trong từng nguyên tố, sau đó xác định số e của ion
+) Số e của ion dương = số e nguyên tử - số đơn vị điện tích
+) Số e của ion âm = số e nguyên tử + số đơn vị điện tích
Lời giải chi tiết:
Na có Z = 11 => số e = 11 => ion Na+ có số e = 11 – 1 = 10
Mg có Z = 12 => số e = 12 => ion Mg2+ có số e = 12 – 2 = 10
Al có Z = 13 => số e = 13 => ion Al3+ có số e = 13 – 3 = 10
Ca có Z = 20 => số e = 20 => ion Ca2+ có số e = 20 – 2 = 18
S có Z = 16 => số e = 16 => ion S2- có số e = 16 + 2 = 18
Cl có Z = 17 => số e = 17 => ion Cl- có số e = 17 + 1 = 18
O có Z = 8 => số e = 8 => ion O2- có số e = 8 + 2 = 10
Vậy có 4 ion có 10e
Câu hỏi 9 :
Cho độ âm điện Ca (1,00), Cl (3,16). Liên kết trong phân tử CaCl2 thuộc loại
- A
liên kết cộng hóa trị có cực.
- B
liên kết ion.
- C
liên kết cho – nhận.
- D
liên kết cộng hóa trị không phân cực
Đáp án: B
Lời giải chi tiết:
∆x = 3,16 – 1 = 2,16 > 1,7 => liên kết ion
Câu hỏi 10 :
Số oxi hóa của N, O, S, Cl, Br, Cr, Mn trong các chất và ion: NH4+, CH3COOH, SO42–, Cl2, KBrO3, K2Cr2O7, K2MnO4 lần lượt là:
- A
+3, –2, +4, 0, +5, +6, +7.
- B
–3, 0, +6, 0, +3, +7, +7.
- C
–3, –2, +6, 0, +5, +6, +6.
- D
–3, –2, +4, 0, +7, +6, +6.
Đáp án: C
Lời giải chi tiết:
\(\overset{-3}{\mathop{N}}\,{{\overset{+1}{\mathop{H}}\,}_{4}}^{+},\text{ }{{\text{C}}_{2}}{{\overset{{}}{\mathop{H}}\,}_{4}}{{\overset{-2}{\mathop{O}}\,}_{2}},\text{ }\overset{+6}{\mathop{S}}\,{{\overset{-2}{\mathop{O}}\,}_{4}}^{2-},\text{ }{{\overset{0}{\mathop{Cl}}\,}_{2}},\text{ }\overset{+1}{\mathop{K}}\,\overset{+5}{\mathop{Br}}\,{{\overset{-2}{\mathop{O}}\,}_{3}},\text{ }{{\overset{+1}{\mathop{K}}\,}_{2}}{{\overset{+6}{\mathop{Cr}}\,}_{2}}{{\overset{-2}{\mathop{O}}\,}_{7}},\text{ }{{\overset{+1}{\mathop{K}}\,}_{2}}\overset{+6}{\mathop{Mn}}\,{{\overset{-2}{\mathop{O}}\,}_{4}}\)
=> Số oxi hóa của N, O, S, Cl, Br, Cr, Mn lần lượt là: -3 ; -2; +6 ; 0 ; +5; +6 ; +6
